L’endométriose est une maladie chronique inflammatoire qui concerne 1 à 2 personnes sur dix ayant un utérus, pouvant provoquer de violentes douleurs, une fatigue chronique, le dysfonctionnement et/ou la perte de l’usage de certains membres et organes, ainsi que l’infertilité. C’est une pathologie complexe à l’origine d’une longue errance diagnostique. Il n’existe aujourd’hui aucun traitement à cette maladie. Certains cas rares d’endométriose peuvent être asymptomatiques.
L’endométriose se caractérise par la présence à l’extérieur de l’utérus de tissu semblable à l’endomètre (l’endomètre est le tissu qui recouvre la paroi interne de l’utérus. Au début de chaque cycle menstruel et sous l’effet des hormones, l’endomètre s’épaissit en vue d’accueillir une potentielle grossesse. Si aucun ovule n’est fécondé en fin de cycle, l’endomètre, qui est un tissu vascularisé, se désagrège et saigne : ce sont les règles). Ce tissu, implanté sur d’autres organes, suit le rythme hormonal : il s’épaissit, se vascularise puis se désagrège et saigne en dehors de l’utérus, c’est l’endométriose. Il est important de préciser que lorsqu’on parle d’endométriose, il s’agit d’un tissu semblable, mais qui n’est pas de l’endomètre à proprement parler.
Ce tissu peut coloniser l’ensemble des organes génitaux : vagin, utérus, trompes, ovaires, ligaments utérins, péritoine (membrane tapissant la cavité abdominale et les organes qui s’y trouvent), l’espace séparant le vagin du rectum, etc.
Il peut également s’étendre à des organes non génitaux : vessie, appendice, côlon, intestin grêle, paroi abdominale, diaphragme (muscle qui sépare le thorax de l’abdomen), plèvre (membrane qui recouvre les poumons), etc.
Tous ces espaces ou organes colonisés ne sont pas, à l’inverse de l’utérus, anatomiquement conçus pour évacuer les saignements. Les cellules, n’ayant pas la possibilité de s’évacuer, se collent aux organes environnants et s’y développent. Peuvent s’ensuivre lésions, nodules, kystes, réactions inflammatoires, formation de cicatrices fibreuses et d’adhérences pouvant accoler les organes avoisinants et provoquer leur dysfonctionnement ou la perte de leur fonction.
Il est difficile de parler de l’endométriose de façon linéaire tant ses formes, symptômes et localisations potentielles sont multiples. On dit d’ailleurs souvent qu’il y a autant d’endométrioses que de personnes atteintes.
L’usage veut aujourd’hui que l’on parle DES endométrioses.
On peut classer les endométrioses en fonction de la localisation des lésions : on parle alors d’endométrioses pelviennes, localisées dans le petit bassin et d'endométrioses extra-pelviennes, en dehors du petit bassin.
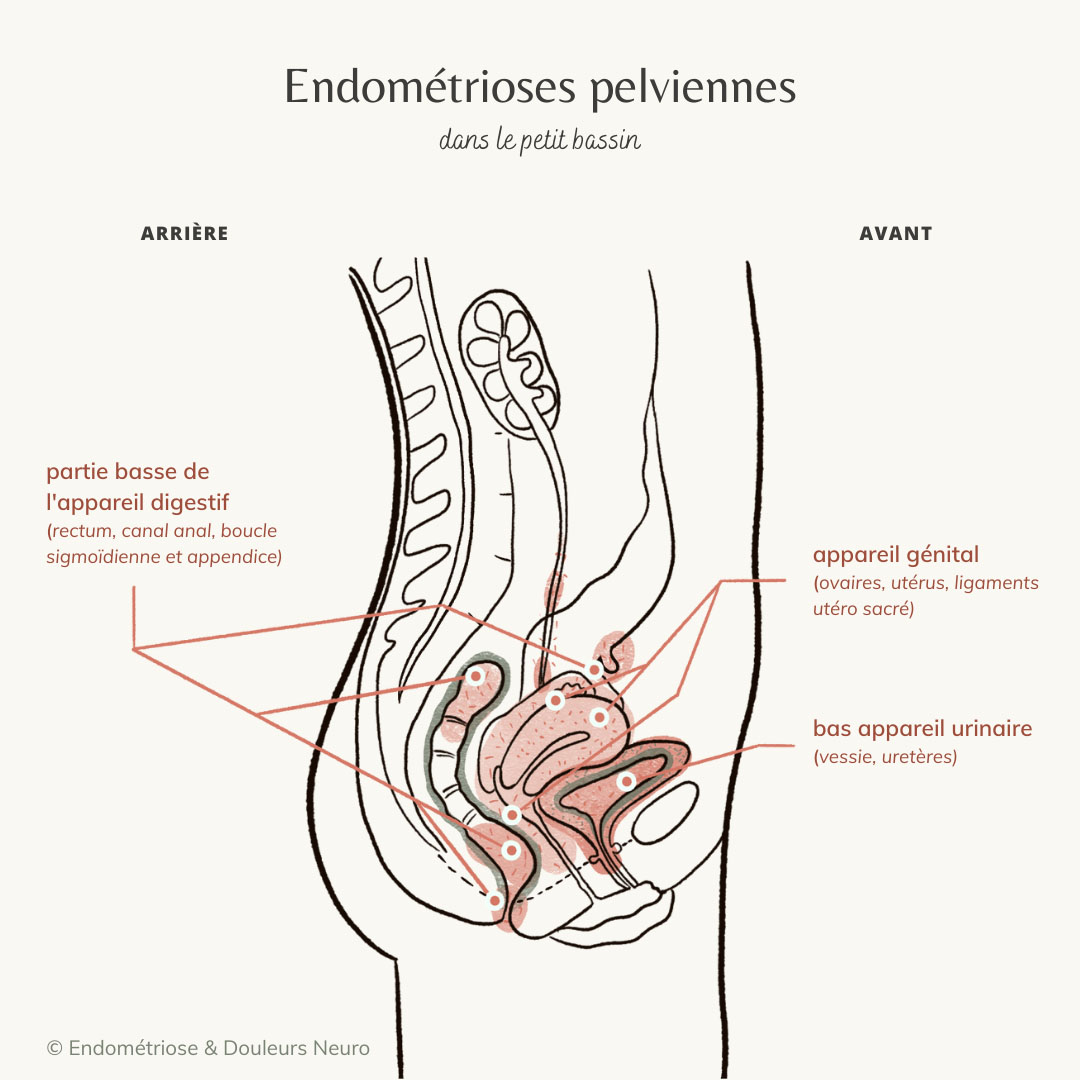

Les atteintes pelviennes vont concerner principalement : le bas de l’appareil urinaire (la vessie, la portion basse des uretères (canaux reliant les reins et la vessie), les reins, l’appareil génital (les ovaires, le muscle interne de l’utérus : on parle alors d’adénomyose, les ligaments utéro-sacrés), une partie de l’appareil digestif (rectum, canal anal et parfois la boucle sigmoïdienne, ainsi que l’appendice), la cloison recto-vaginale, le cul-de-sac de Douglas.
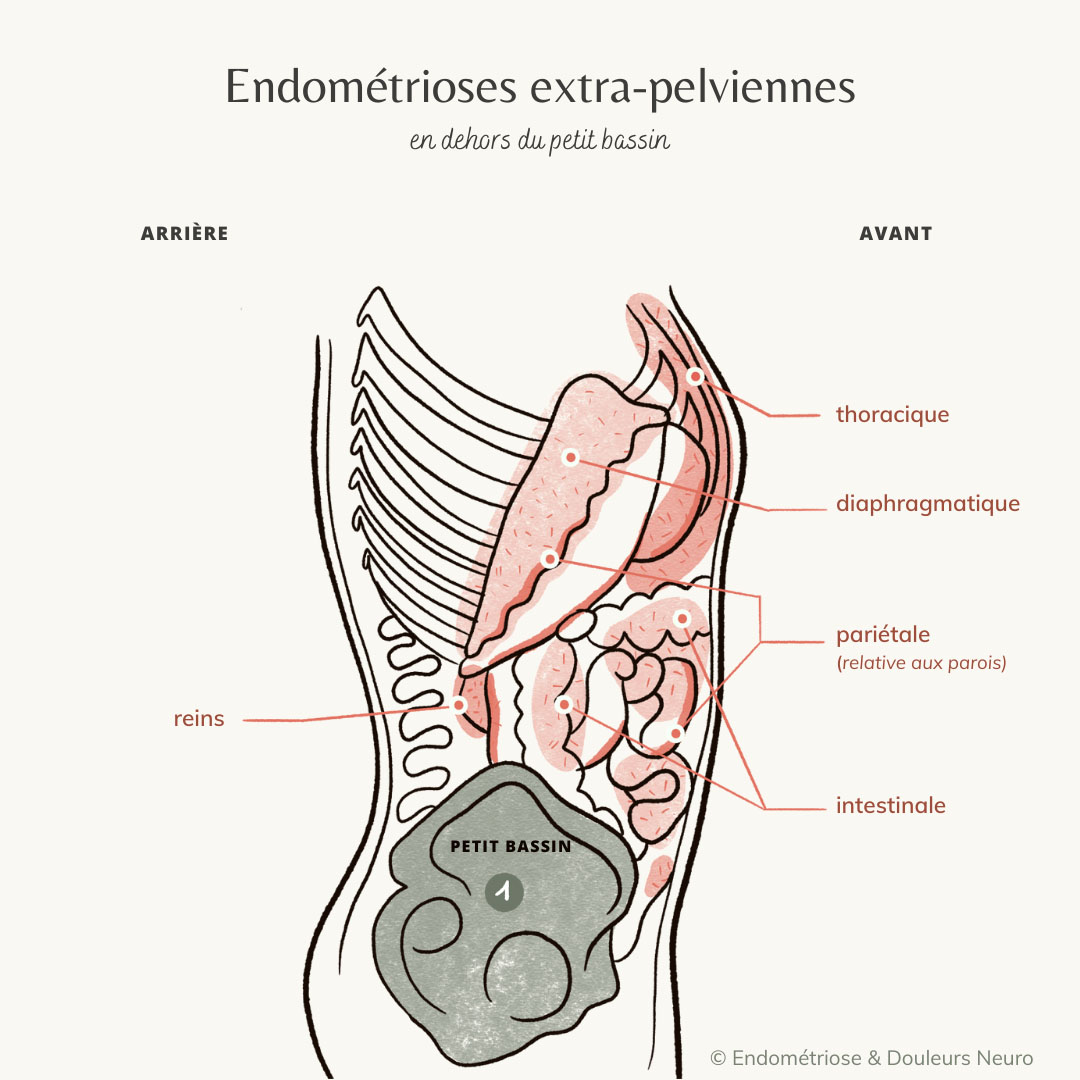
S’agissant des atteintes extra-pelviennes, elles peuvent toucher les intestins, le diaphragme, le thorax, la paroi abdominale (atteintes pariétales). Cette liste est non exhaustive.
L’endométriose est loin d’être une « simple » maladie gynécologique. C’est une maladie systémique qui peut se développer partout dans le corps et peut avoir des conséquences sur de multiples aspects de la vie de la personne atteinte.
Malgré ce que l’on peut entendre, l’endométriose ce n’est pas « des douleurs de règles »... ou du moins pas seulement !
En rapport avec le système gynécologique :
En rapport avec le système digestif :
En rapport avec le système nerveux et la forme physique :
Le fait d’être atteint·e d’endométriose peut engendrer des conséquences comme :
L’endométriose est aujourd’hui classée selon 3 formes :
Précisons qu'au-delà de ces 4 formes principales énoncées, il existe plein de types d'endométrioses, au niveau du diaphragme ou du cerveau par exemple.


Les endométrioses sont très variées et seront différentes d’une personne à une autre.
Pour s’y retrouver, les médecins ont souvent classé les endométrioses selon des « stades ».
Cela fait référence à une classification de l’American Fertility Society publiée en 1978 (révisée en 1995 & 2017) pour évaluer une endométriose selon la localisation des lésions, leur taille et leur profondeur. Ce système de points permet de classer une endométriose sur une échelle de stades de 1 (minime) à 4 (sévère).
Cette échelle n’est plus vraiment utilisée aujourd’hui du fait de l’absence de corrélation entre l’étendue des lésions et les douleurs ressenties. Une personne avec une endométriose de stade 1 peut souffrir plus qu’une personne avec une endométriose de stade 4 par exemple. Cette absence de corrélation étant aujourd’hui démontrée, la notion de stades devient peu représentative. En outre, ce score est uniquement descriptif, sa valeur pronostique est faible et ne permet malheureusement pas de définir l’impact réel ou les douleurs que subissent les personnes atteintes. Il n’y a donc pas de règles à ce sujet. De plus, un même stade peut correspondre à des lésions très différentes.
Si l'on tend à parler de l'endométriose comme étant une maladie multifactorielle, c'est parce que son étiologie (sa cause précise) reste jusqu'à présent inconnue et différentes hypothèses coexistent par ailleurs, afin d'expliquer sa genèse, son mécanisme de formation.
Une première hypothèse est celle du reflux menstruel, dite « théorie de l'implantation ».
Il s'agit de l’implantation de matériel utérin provenant de menstruations rétrogrades (le sang des règles pouvant remonter par les trompes et parvenir à la cavité abdominale, transportant avec lui des fragments d’endomètre).
Cependant, les clinicien-ne-s estiment que 90% des femmes présentent des saignements rétrogrades. Or, seuls 10% de ces femmes développent des lésions d’endométriose (cellules ectopiques : cellules se développant en dehors de leur place habituelle). L’explication est donc, au moins, insuffisante. Dès lors, les scientifiques parlent de facteurs de susceptibilité individuelle.
Il existe par ailleurs plusieurs hypothèses « métaplasiques ». La métaplasie désigne la transformation d'un tissu différencié en un autre tissu différencié.
L'une de ces hypothèses, exposée dès 1987 par le Dr David Redwine, stipule que la mülleriose serait la cause de l’endométriose, qui résulterait alors d'une anomalie dans l’organogenèse du fœtus. L’endométriose serait donc préexistante, présente à l’état embryonnaire, et cela bien avant les premières règles. Elle deviendrait symptomatique dès les premiers cycles. Le tissu embryonnaire présent dans le péritoine pourrait, en effet, former de l’endométriose. Cette théorie sera complétée par d’autres spécialistes au milieu des années 1980, notamment le Dr Ronald Elmer Batt et le Pr Pietro Signorile. Marie-Rose Galès, dans son ouvrage Endométriose : ce que les autres pays ont à nous apprendre paru en 2020, expose notamment cette théorie métaplasique et le retard dans la compréhension et l’utilisation de la bonne définition de l’endométriose en France.
Une dernière hypothèse est celle de la « dissémination » ou de la « métastase », qui suggère que, au moment des règles, les cellules endométriales sont aspirées par les vaisseaux et essaiment dans tout l'organisme via la circulation systémique.
Pour avancer dans ces recherches et dans la compréhension de la maladie, plusieurs projets épidémiologiques ont vu le jour en France sous l’impulsion de l’équipe de Marina Kvaskoff, épidémiologiste et chercheuse à l’INSERM, notamment le projet @compareendo qui étudie le vécu et l'évolution de la maladie auprès des personnes atteintes grâce à des questionnaires en ligne.
Concernant les facteurs de susceptibilité de l'endométriose, les scientifiques étudient aujourd'hui plusieurs pistes :
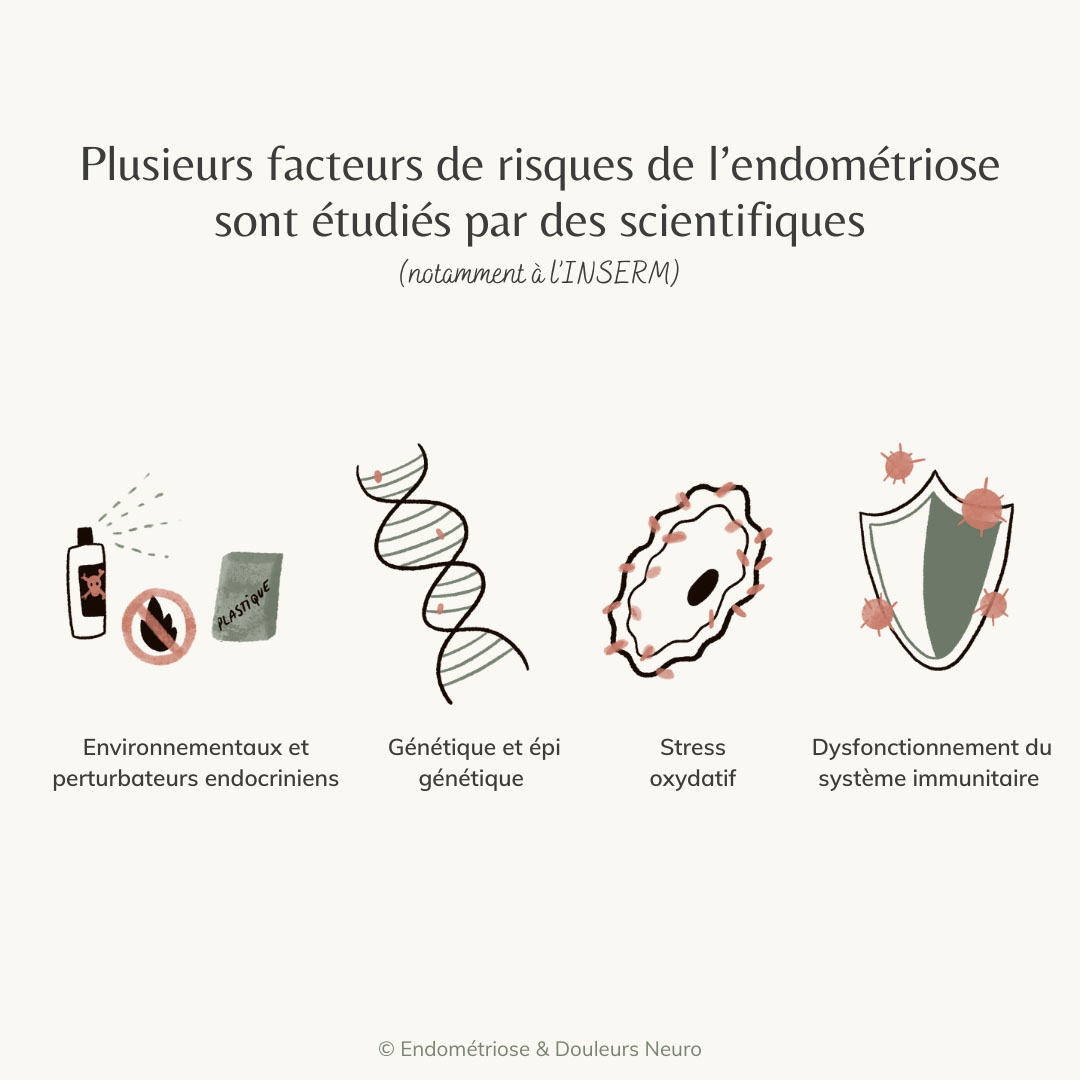
Nous espérons que ces recherches permettront de faire avancer les choses et de mieux comprendre ou même soigner l'endométriose.
Lorsque l’endométriose devient neuropathique, plusieurs nerfs pelviens peuvent être atteints par l’inflammation. Parmi ceux-là, on retrouve le fameux nerf honteux, ou nerf pudendal.
Au sein du faisceau neurovasculaire pudendal, on trouve l'artère, la veine et le nerf pudendal : celui-ci est l’un des plus profonds et difficiles d’accès du schéma neuronal. Il prend sa source dans la moelle épinière, très exactement dans le plexus pudendal au niveau de la troisième racine sacrée du sacrum (S3). Des branches parentes émergeant des deuxième et quatrième racines le rejoignent pour se glisser immédiatement sous le muscle piriforme.
Cette arborescence sort ensuite du bassin et passe près de l’épine sciatique pour confluer et ne former plus qu’un vers les bords supérieurs du ligament sacro-tubéreux et du muscle ischio-coccygien.
Il termine sa course dans un canal fibreux nommé canal d’Alcock (dédoublement de l’aponévrose du muscle obturateur). De là, il donnera naissance à trois nouvelles branches :
Toute la complexité et la spécificité du nerf pudendal réside dans le fait qu’il a un triple rôle : sensoriel, moteur et végétatif. Sensoriel et moteur en innervant les structures somatiques comme les muscles, nous permettant une certaine maîtrise des muscles du plancher pelvien. A contrario, les structures végétatives fonctionnent en toile de fond (comme le cœur, les poumons par exemple). Grâce à cela, le nerf pudendal garantit le maintien d’un tonus des muscles du plancher pelvien, nous permettant, entre autres, de ne pas être incontinent·e·s.
C’est cette autonomie partielle qui peut poser problème lorsque la douleur frappe et perturbe le système nerveux sympathique. Les patient·e·s touché·e·s par la maladie expérimentent divers symptômes évolutifs : augmentation du rythme cardiaque, diminution de mobilité du gros intestin, vasoconstriction des vaisseaux sanguins, dilatation des pupilles, transpiration excessive, augmentation de la pression sanguine, chair de poule, agitation certaine, anxiété… de quoi complexifier le diagnostic et favoriser l’errance médicale des patient·e·s.
La névralgie pudendale dans le cadre de l’endométriose se caractérise le plus généralement par une irritation des petits nerfs du pelvis due à l’irradiation de l’inflammation chronique. Ceux-ci ne savent plus comment réagir et envoient des signaux de douleur au cerveau alors qu’ils ne sont pas endommagés.
En cas d’évolution de la maladie, des lésions d’endométriose peuvent comprimer ou infiltrer les nerfs, dont le pudendal.
On retrouve alors deux types de lésions :
Ces douleurs se traduisent de plusieurs façons en termes de ressenti. Tout d’abord les douleurs spontanées qui se manifestent généralement par une sensation de brûlure dans la zone rectale, périnéale, urétrale et/ou du clitoris et vagin, ainsi que dans les cuisses lors de fortes crises.
Les endométriosiques peuvent également vivre un Accès Douloureux Paroxystique (ADP), une crise de douleurs soudaine et aiguë qui peut durer plusieurs heures : sensation de corps étranger au niveau du rectum (balle de tennis), picotements/décharges électriques/sensation d’aiguilles et pincements, torsions ou tiraillements dans tout le périnée sont au programme. Ces crises surviennent généralement suite à une stimulation extérieure : frottements contre la peau, station assise/debout prolongée, trop forte mobilisation physique, changements soudains de température dans les extrêmes.
Un problème n’arrivant jamais seul, des dommages collatéraux surviennent dès le début de l’atteinte. On retrouve en premier lieu les problèmes urinaires et fécaux : sensation de brûlure à la miction, cystite interstitielle, dysurie (difficultés mictionnelles), petites fuites post-miction, douleurs à la défécation avec diarrhées et/ou constipations qui peuvent évoluer vers un Syndrome du Côlon Irritable.
Apparaissent aussi la plupart du temps des troubles sexuels : douleurs durant et/ou après les rapports/à la pénétration, absence de plaisir et libido en berne, hypersensibilité au niveau du clitoris et de la vulve.
Bien qu’ayant des causes différentes, les deux termes sont souvent confondus et établis comme synonymes.
La compression du nerf pudendal est définie par le blocage physiologique du nerf nécessitant une intervention chirurgicale pour le libérer. Cette compression peut provoquer des névralgies pudendales mais a contrario, les névralgies pudendales ne peuvent pas créer de compression des nerfs. On sait aujourd’hui qu’il y a principalement trois causes à cette pathologie : une malformation de naissance (canal d’Alcock rétréci par exemple), une activité sportive répétée (cyclisme, équitation) qui aura pu créer de micros lésions et des atteintes suite à une opération dans la région pelvienne. Ainsi, dans le cadre de l’endométriose, de nombreux·ses chirurgien·ne·s font aujourd’hui marche arrière et ne conseillent l’opération qu’en dernière intention car au-delà de la possible multiplication de fibrose suite à la cicatrisation (pouvant ainsi immobiliser les organes, tirer les nerfs et perturber leur signal), il y a toujours un risque de section de nerfs, surtout si l’opération est menée par un·e chirurgien·ne non formé·e en neuropelvéologie (spécialité en plein essor se concentrant sur les pathologies du système nerveux pelvien).
Le terme « compression du nerf pudendal » ou « Pudendal Nerve Entrapment » est apparu dans la littérature scientifique européenne dès les années 80 avec le développement des traitements de blocage de groupes de nerfs (« nerve blocks ») et des chirurgies de décompression.
L’un des symptômes principaux de la compression du nerf pudendal étant des douleurs lors de la station assise, comme pour les névralgies pudendales, les deux termes ont rapidement été confondus, ainsi que les traitements possibles. La chirurgie devint la réponse quasi systématique, à tort.
Les protocoles (nerve blocks, traitements et kinésithérapie) se sont avérés inefficaces chez certain·e·s patient·e·s car se concentrant sur les conséquences de la douleur et non la cause réelle. Ajoutant à cela l’errance médicale qui a pour conséquence l’intégration de la douleur par le système nerveux, les médecins se retrouvaient avec des patient·e·s intraitables.
Le diagnostic évolua grâce aux découvertes autour du syndrome myofascial ainsi qu'à une approche pluridisciplinaire des traitements comme appliquée aujourd’hui.
De même, les progrès autour des méthodes de détection employées ont mis en évidence qu’il est impossible de savoir si le/la patient·e souffre d’une compression du nerf pudendal avant d’opérer. C’est d’ailleurs le constat d’un soulagement de la douleur en post-opératoire qui permet d’affirmer qu’il y avait bien compression du nerf pudendal (selon les recherches du Professeur Roger Robert, du Docteur J.J. Labat et de leurs équipes).
Bien que la névralgie pudendale soit aujourd’hui reconnue, sa découverte reste récente. La méconnaissance du sujet par le corps médical et les symptômes, trop divers et variés, sont autant de facteurs qui ne permettent pas un diagnostic rapide. L’errance médicale qui en résulte peut entraîner de lourdes conséquences, aussi bien en termes de prise en charge (mauvais traitements pouvant aggraver la situation, évolution de la maladie jusqu’à en devenir irréversible) que sur le plan psychologique (incapacité à travailler/sortir menant à un isolement social, abandon de la vie sexuelle, dépression, suicide).
Les examens de première intention (radio, scanner, IRM) ne permettent pas de détecter les nerfs et leur état, mais ils sont cependant nécessaires pour éliminer d’autres pathologies comme le syndrome de la queue de cheval. Dans le cadre de l’endométriose, une IRM pelvienne s'avère indispensable, mais d’autres IRM peuvent également être intéressantes (lombaire, sacro-iliaque).
Si exercé par un·e praticien·ne averti·e, un examen physique peut être effectué et apporter un éclairage nouveau sur le diagnostic, là où l’exploitation des imageries aurait pu se révéler infructueuse. Appelé « Signe de Tinel », l’acte consiste en de petits tapotements autour du nerf pour générer une sensation de pincements et d’aiguilles.
Une autre méthode, via un touché rectal ou vaginal, permet d'observer une douleur vive autour de l’épine ischiatique/le bord médial de l’ischion, région où le nerf pudendal passe. Des douleurs autour du muscle piriforme et du coccyx sont également assez courantes.
Ceci étant dit, le diagnostic de la névralgie pudendale se base aujourd’hui principalement sur l’historique médical du/de la patient·e, de son vécu et de ses symptômes. Pour cela, le corps médical peut s’appuyer sur les « critères de Nantes » : lorsqu’il constate que les quatre critères cliniques indispensables (douleurs dans le territoire du nerf pudendal, aggravées en position assise, ne réveillant pas la nuit et sans hypoesthésie objective) sont réunis, on peut raisonnablement penser à une névralgie pudendale.
Le questionnaire DN4, qui traite des douleurs neuropathiques en général, peut également s’avérer utile.
L’ENMG (électroneuromyogramme), qui est souvent mis en avant quand on parle d’atteintes aux nerfs, ne permet pas, en réalité, de faire la distinction entre une névralgie pudendale ou une compression du nerf. Il mesure l’efficacité du trajet nerveux sur l’ensemble des nerfs périphériques et permet ainsi de détecter les nerfs défaillants. Cependant, il a été démontré que cette pratique, en plus d’être désagréable voire douloureuse, peut présenter des faux positifs ou négatifs, surtout chez les personnes ayant accouché. De plus, la névralgie pudendale ou la compression du nerf pudendal sont des pathologies sensorielles : ce test mesure la rapidité des fibres motrices et non l’intensité de la douleur. Sa prescription est donc loin d’être systématique et n’est que très peu pratiquée en France (seulement deux spécialistes).
Reste, enfin, la question complexe du traitement.
Une fois le diagnostic posé, un protocole est mis en place pour soulager le/la patient·e. « Soulager » est un mot important car en cas d’inflammation des nerfs suite à une endométriose, les nerfs concernés ne pourront pas être “guéris” si on ne traite pas la racine du problème : l’inflammation. De même, si, malheureusement, les nerfs sont abîmés, voire détruits par l’endométriose, ils seront difficiles voire impossibles à réparer. La névralgie pudendale est donc un problème largement sous-estimé et très sérieux dans ce contexte car pouvant conduire à des dommages irréversibles et handicapants à vie.
Dans la boîte à outils disponible pour lutter contre la névralgie pudendale, on retrouve un large panel de solutions, adaptables selon la source et la gravité de l’atteinte :
Dans les traitements de médecine « douce », on retrouve également :
Notre contenu est à visée strictement informative et ne saurait remplacer vos relations avec un·e professionnel·le de santé.